《细胞》子刊:高脂饮食三天就能洗脑!
来源:奇点网
就在刚刚,我突然涌上了一股吃炸鸡的冲动。这使我掏出手机开始浏览外卖平台,并且心里暗暗打算等会儿要去超市买瓶啤酒配上。
然后我又撇了一眼刚看完的这篇论文,戳手机的指头有那么一丝丝颤抖。
近期,《细胞代谢》杂志发表了一项来自耶鲁大学科学家的研究[1]。研究者们发现,高脂饮食会诱导大脑的变化,刺激下丘脑产生炎症,并诱导机体摄入更多的热量,最终导致体重增加。这种变化来得很快,三天高脂饮食之后就会出现,甚至发生在身体变胖之前。
令人惊讶的是,大脑变化的直接操盘手,竟然是我们颇为熟知的小胶质细胞。要知道小胶质细胞主管的是免疫功能,参与代谢调控,这手可伸得有点儿长。

其实有很多研究已经证明了中枢神经在能量和糖代谢中的重要作用,它会响应循环内的各种信号一一做出回应,比如瘦素,胰岛素等激素,又比如葡萄糖和脂肪酸等营养物质[2]。
在整个儿中枢神经系统中呢,下丘脑又显得尤为突出,是控制新陈代谢的指令中心。科学家们已经在下丘脑中鉴定到了几个特别的神经元群,认为他们是外周代谢的重要传感器和调节因子[3]。
不过比较关注神经科学的读者一定知道,大脑中神经元只占一半儿,另一半的神经胶质细胞们近年也逐渐取得了科学家的重视,它们在体重平衡和肥胖中也有自己的角色[4]。
根据细胞起源,胶质细胞一般可以被分为大胶质细胞,星形胶质细胞,少突胶质细胞和小胶质细胞,目前我们一般认为小胶质细胞就相当于中枢神经系统里的巨噬细胞,主要发挥免疫作用。
但是这个认知却被今天这项研究给狠狠刷新了一下。具体怎么回事儿,咱们先从“胖”说起。

此前就有科学家发现,吃多变胖这回事儿,是先从脑子开始的。在饮食诱导肥胖这个过程中,高脂/高碳水饮食开始3天后,就发现了下丘脑炎症和胶质增生,而此时,实验动物的体重甚至还没来得及增加[5]。同时,下丘脑中的小胶质细胞也被激活了。
被激活的小胶质细胞中,有一种蛋白UCP2表达水平非常高。UCP2是一种线粒体蛋白,是线粒体功能的重要组成部分。
小胶质细胞本身是非常“活跃”的细胞。这个活跃就是字面意思,它们能够迅速改变形状,向受损伤部位迁移,并开启吞噬功能。这几个过程都需要不少能量,所以线粒体代谢改变也算是常规操作[6]。
其实到这里为止事情还是挺平常的。高脂饮食诱导炎症,有炎症所以小胶质细胞出动,要工作所以线粒体加班,不用细想都觉得正常。
那么接下来就来看看今天这项研究的发现吧。

第一步当然是先给小鼠的菜单安排上。对照组小鼠吃的是标准鼠粮(SD),三个实验组的高脂饮食(HFD)则分别进行了3天,7天和8周。
当检测下丘脑中小胶质细胞的线粒体变化,有趣的事情发生了。3天高脂饮食使小胶质细胞中的线粒体变得更小了,但是同时数量却变多了,另外三组呢,可以认为没变化,基本差不多。与这些变化一致的是,只有3天组UCP2表达水平显著升高了。

可见3天组线粒体数量增加
研究者还另外测定了一些炎性细胞因子的水平,结果也很有趣。在3天和7天组中细胞因子水平都比较高,但是8周组反而回落了。详细的数值可以看下图。
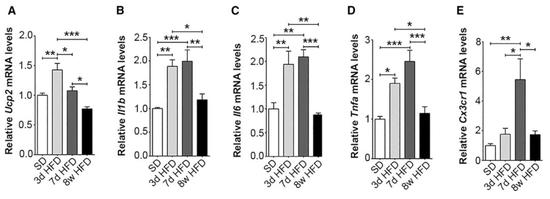
结果真的很有说法
当研究者敲除小鼠的UCP2基因,高脂饮食就不再能影响到大脑了,3天后小鼠下丘脑胶质细胞中的线粒体并没有什么变化。

敲除UCP2之后线粒体基本无变化
更棒的是,敲除了UCP2之后,小鼠好似对高脂饮食产生了“抗性”,它们吃得更少,每天消耗的能量更多,自然体重也增长得更慢了。除此之外,小鼠的糖耐量和胰岛素敏感性也有所改善,这是与代谢表型整体好转有关的。
另外,有趣的是,在运动能力,瘦体重等更细一步的指标上,雄性小鼠和雌性小鼠表现出了明显的差异。这可能是因为性别带来的激素水平差异导致的吧。
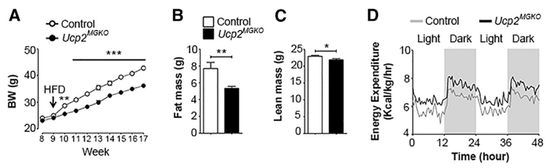
小鼠体重增长,胖/瘦体重,能量消耗
那么为什么搞定了UCP2,高脂饮食就不能作妖了呢?
啧啧啧,小胶质细胞这个浓眉大眼的好同志,竟然在这里坑了我们一把。
高脂饮食之后,被激活的小胶质细胞居然会激活POMC神经元。这个POMC神经元,简单说来就是管理我们想吃什么想吃多少的神经元[4],所以说,是小胶质细胞让我们吃了高脂饮食还想吃(吃成一个小胖子)。
但在缺失UCP2的情况下,这种机制就被阻断了。
So,小胶质细胞不光是执行免疫功能,还配合饮食帮我们变胖啊~
从进化的角度来看,这在当年物质还比较匮乏的时候应该是个蛮有用的机制。有吃的的时候就多吃点儿~长胖点儿~不过现在我们已经不差吃的了,或者说是吃得已经太多了。
求小胶质细胞跟上时代,不要再搞怪了。
参考资料:
[1]https://www.cell.com/cell-metabolism/fulltext/S1550-4131(19)30439-5
[2] Sandoval, D.A。, Obici, S。, and Seeley, R.J。 (2009)。 Targeting the CNS to treat type 2 diabetes。 Nat。 Rev。 Drug Discov。 8, 386–398。
[3] Horvath, T.L。, Diano, S。, and Tscho¨ p, M。 (2004)。 Brain circuits regulating energy homeostasis。 Neuroscientist 10, 235–246。
[4] Horvath, T.L。, Sarman, B。, Garca-Ca ceres, C。, Enriori, P.J。, Sotonyi,江苏农林职业技术学院教务处 P。, Shanabrough, M。, Borok, E。, Argente, J。, Chowen, J.A。, Perez-Tilve, D。, et al。 (2010)。 Synaptic input organization of the melanocortin system predicts diet-induced hypothalamic reactive gliosis and obesity。 Proc。 Natl.Acad。 Sci。 USA 107, 14875–14880。
[5] Thaler, J.P。, Yi, C.X。, Schur, E.A。, Guyenet, S.J。, Hwang, B.H。, Dietrich, M.O。, Zhao, X。, Sarruf, D.A。, Izgur, V。, Maravilla, K.R。, et al。 (2012)。 Obesity is associated with hypothalamic injury in rodents and humans。 J。 Clin。 Invest。 122, 153–162。
[6] Rose, J。,江苏农林职业技术学院教务处 Brian, C。, Woods, J。, Pappa, A。, Panayiotidis, M.I。, Powers, R。, and Franco, R。 (2017)。 Mitochondrial dysfunction in glial cells: implications for neuronal homeostasis and survival。 Toxicology 391, 109–115。
本文作者 | 代丝雨






